Kwaksalwer
Erscheinungsbild
(Widjerfeerd faan Quecksilber)
| Eegenskapen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Algemian | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nööm, Symbool, Numer | Kwaksalwer, Hg, 80 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Seerie | Auergungsmetal | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skööl, Periode, Blook | 12, 6, d | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klöör, Skak | salwern witj | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS-Numer | 7439-97-6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ATC-Code | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Uundial | 0,4 ppm[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomaar [2] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atoommase | 200,592(3)[3] u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atoomraadius (bereegent) | 150 (171) pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalent-Raadius | 132 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waals-Raadius | 155 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektroonen | [Xe] 4f14 5d10 6s2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energii | 4,49 eV[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1. Ionisiarang | 1007,1 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2. Ionisiarang | 1810 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Füsikaalisk [2] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tustant | luupen | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sachthaid | 13,5459 g/cm3[5] bei 293,15 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hardhaid | entfällt | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetismus | diamagneetisk (Χm = −2,8 · 10−5)[6] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Smoltponkt | 234,32 K (−38,83 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Köögponkt | 630,2 K[7] K (357 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molaar Rüm | (fest) 14,09 · 10−6 m3/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dampwaremk | 58,2 kJ/mol[7] kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Smoltwaremk | 2,37[8] kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dampdruk | 0,163[5] Pa bei 293 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Faard faan a tuun | 1407 m/s bi 293,15 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Waremk | 140 J/(kg · K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrisk struumfeerang | 1,04 · 106 A/(V · m) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Waremkfeerang | 8,3 W/(m · K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cheemisk [2] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oksidatsionstustant | 1, 2, 4[9] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oksiiden | Hg2O, HgO | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sür of baasisk | lacht baasisk | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Normoolpotentiaal | 0,8535 V (Hg2+ + 2 e− → Hg) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegatiwiteet | 2,00 (Pauling-Skala) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotoopen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Muar isotoopen bi List faan isotoopen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NMR-Eegenskapen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Seekerhaid | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Muar wäärnangen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| MAK-miat | Sweits: 0,005 ml·m−3 bzw. 0,05 mg·m−3[11] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Miast wurd SI-ianhaiden brükt. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Kwaksalwer (ualgreks ὑδράργυρος Hydrargyros ,luupen salwer‘) as en cheemisk element mä det ufkörtang Hg an det atoomnumer 80. Hat as det iansagst luupen metal an böös giftag.
Bilen
[Bewerke | Kweltekst bewerke]-
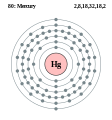
Elektroonenskel
-
Rian kwaksalwer
-
Kwaksalwer uun en gasröör
-
En manomeeter mä kwaksalwer
-
En baromeeter
-
En termomeeter
Luke uk diar
[Bewerke | Kweltekst bewerke]Kwelen
[Bewerke | Kweltekst bewerke]- ↑ Harry H. Binder: Lexikon der chemischen Elemente. S. Hirzel Verlag, Stuttgart 1999, ISBN 3-7776-0736-3.
- ↑ A taalen för't infobox kem miast faan www.webelements.com (Quecksilber) .
- ↑ CIAAW, Standard Atomic Weights Revised 2013.
- ↑ Ludwig Bergmann, Clemens Schaefer, Rainer Kassing: Lehrbuch der Experimentalphysik. Band 6: Festkörper. 2. aplaag. Walter de Gruyter, 2005, ISBN 3-11-017485-5, S. 361.
- ↑ 5,0 5,1 5,2 5,3 Iindraanj tu Quecksilber uun't GESTIS-dootenbeenk faan't IFA, ufrepen di 11. Januar 2010 (mä JavaScript).
- ↑ Robert C. Weast (Hrsg.): CRC Handbook of Chemistry and Physics. CRC (Chemical Rubber Publishing Company), Boca Raton 1990, ISBN 0-8493-0470-9, S. E-129 bit E-145. Wäärser diar uun g/mol an uun cgs-ianhaiden. Heer amreegent tu SI-wäärs.
- ↑ 7,0 7,1 Yiming Zhang, Julian R. G. Evans, Shoufeng Yang: Corrected Values for Boiling Points and Enthalpies of Vaporization of Elements in Handbooks. Uun: Journal of Chemical & Engineering Data. 56, 2011, S. 328–337, doi:10.1021/je1011086.
- ↑ M. Simon, P. Jönk, G. Wühl-Couturier, S. Halbach: Mercury, Mercury Alloys, and Mercury Compounds. In: Ullmann’s Encyclopedia of Industrial Chemistry. Wiley-VCH Verlag, Weinheim 2006, doi:10.1002/14356007.a16_269.pub2.
- ↑ Xuefang Wang, Lester Andrews, Sebastian Riedel, Martin Kaupp: Mercury Is a Transition Metal: The First Experimental Evidence for HgF4. Uun: Angewandte Chemie. 119, 2007, S. 8523–8527, doi:10.1002/ange.200703710.
- ↑ Iindrach tu Mercury uun't Classification and Labelling Inventory faan't Europeesk Chemikaalienagentuur (ECHA), ufrepen di 1. August 2016.
- ↑ Schweizerische Unfallversicherungsanstalt (SUVA): Aktuel MAK- an BAT-wäärser